
Νίκος Καλλιακμάνης
Η M.G. είναι μη οργάνων ειδική* αυτοάνοση νόσος, συστηματική νόσος.
*Μη οργάνων ειδική : Τα υπάρχοντα αυτά αντισώματα δεν στρέφονται κατά ενός οργάνου – ιστού.
Η M.G. χαρακτηρίζεται από ύπαρξη αντισωμάτων κατά των υποδοχέων της ακετυλοχολίνης μέσω των οποίων φυσιολογικά μεταβιβάζεται το νευρικό ερέθισμα προς την τελική κινητική πλάκα με επακόλουθο την κίνηση του μυός (βλέπε Εικόνα 1, Εικόνα 1α).
Εικόνα 1
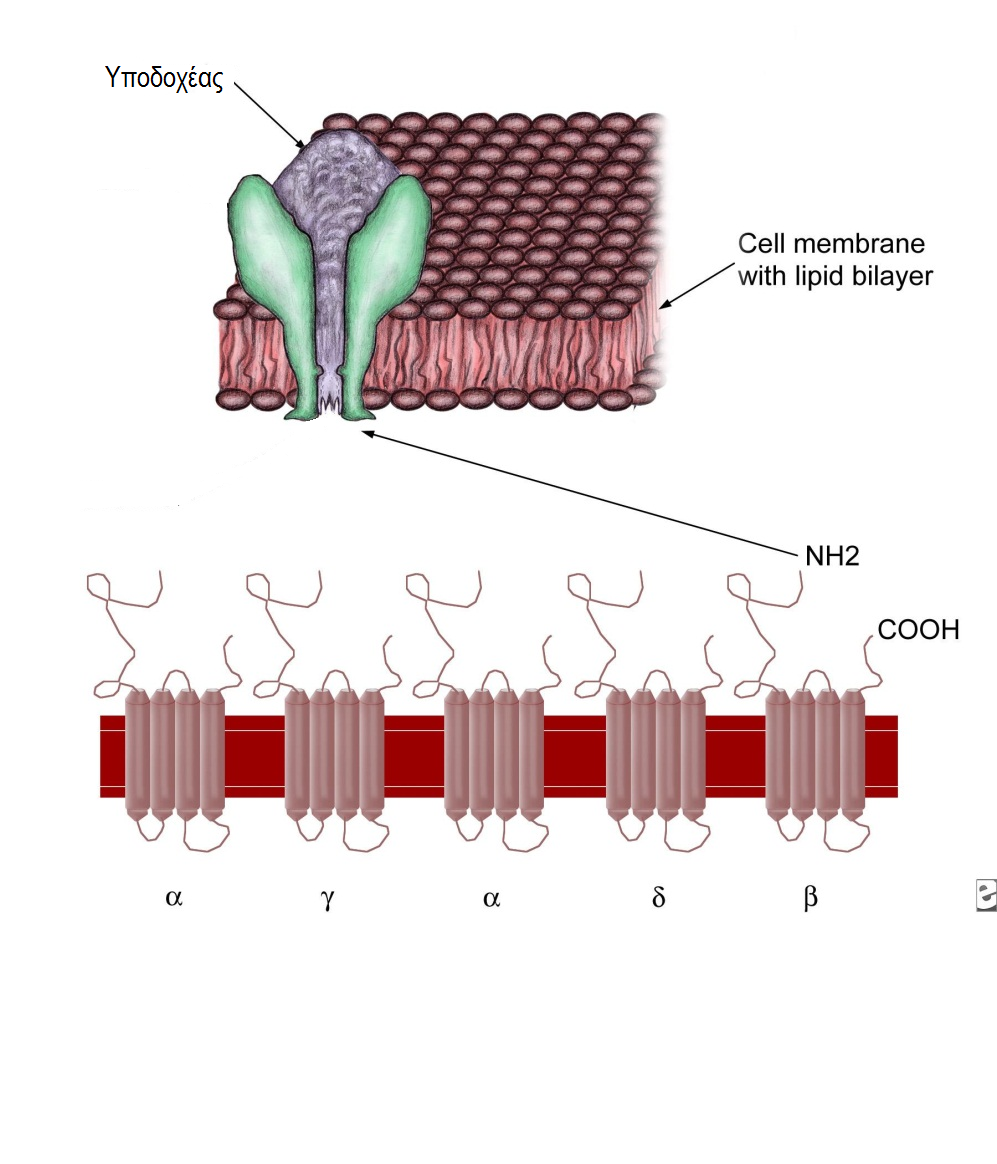
Υποδοχέας Ακετυλοχολίνης – 5 υποομάδες κάθε μία με μορφή «ροζέτας» με κεντρικό άνοιγμα → κανάλι ιόντων
Εικόνα 1α
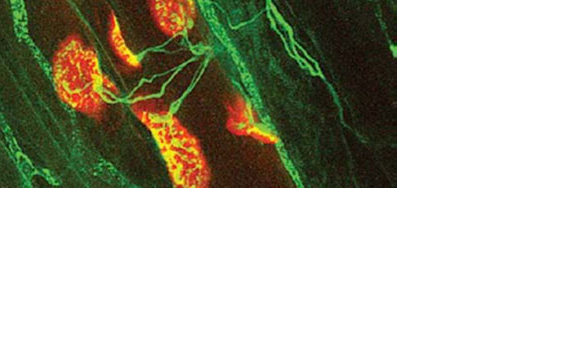
Νευρομυική σύναψη. Αναοσοιστοχημική αποτύπωση μυός στη περιοχή της ννευρομυικής σύναψης, όπου φαίνονται οι απολήξεις των νεύρων (πράσινο) που καταλήγουν στη περιοχή της σύναψης, που είναι πλούσια σε υποδοχείς της ακετυλοχολίνης (κόκκινο χρώμα).
Το τελικό αποτέλεσμα στη M.G. είναι η λειτουργική μείωση του αριθμού των υποδοχέων αυτών με προοδευτική μείωση της μυϊκής ισχύος ειδικά μετά από επαναλαμβανόμενες κινήσεις όπως και η μείωση φυσιολογικής ισχύος μυός μετά από περίοδο ανάπαυσης.
Επίσης υπάρχουν (λιγότερο συχνά) αυτοαντισώματα κατά των υποδοχέων της κινάσης της τυροσίνης* (Muscle Specific Tyrosine Kinase – MUSK) των μυών (οι υποδοχείς αυτοί είναι απαραίτητοι για τη λειτουργία της νευρομυϊκής σύνθεσης).
*Κινάση της τυροσίνης : Αποτελεί χημικό προϊόν του κυττάρου, παίζει κεντρικό ρόλο στη διαίρεσή του, ενεργοποιώντας το στάδιο μίτωσης στον κάθε κυτταρικό κύκλο. Υποδοχείς που συνδέονται με την κινάση της τυροσίνης αποτελούν διαμεμβρανικούς υποδοχείς (η μία απόληξη βρίσκεται εκτός του κυττάρου και εκεί επιτελείται η σύνδεση ουσίας, φαρμάκου, και την άλλη απόληξη εντός του κυττάρου ευρισκόμενη, συνδεμένη με κινάση).
*Νικοτινικοί Υποδοχείς Ακετυλοχολίνης : Πρέπει να σημειωθεί ότι απαντώνται σε όλους του ιστολογικούς τύπους Ca πνεύμονα. Είναι «πενταμερείς δίαυλοι» που επιτρέπουν τη διέλευση ιόντων Na, Ca (βλέπε εικόνα).
3 ΤΥΠΟΙ ΥΠΟΔΟΧΕΩΝ ΑΚΕΤΥΛΟΧΟΛΙΝΗΣ ΥΠΑΡΧΟΥΝ
Α) ΝΙΚΟΤΙΝΙΚΟΙ : Γάγγλια αυτόνομου (Ν1) – κύτταρα επινεφριδίων – κινητικές πλάκες σωματικού Ν.Σ. Όταν διεγείρονται προκαλούνται συσπάσεις γραμμωτών μυών, αύξηση πίεσης, έκκριση κατοχολαμίνων από μυελό επινεφριδίων, υπεργλυκαιμία.
Β) ΜΟΥΣΚΑΡΙΝΙΚΟΙ : (Μx) : Τελικοί αποδέκτες των μεταγαγγλιακών παρασυμπαθητικών ινών. Εντοπίζονται στα όργανα στόχους που νευρώνονται από μεταγαγλλιακές παρασυμπαθητικές ίνες και προκαλούν στους καρδιακούς μύς – αδένες – αύξηση εκκρίσεων σιελογόνων, ιδρωτοποϊών, δακρυϊκών – ΓΕΣ (αύξηση περισταλτισμού) – σύσπαση ουροδόχου κύστης – εγκύμονος μήτρας – βρόγχων – βραδυκαρδία – Αρτηριακή Υπέρταση.
Γ) ΝΙΚΟΤΙΝΙΚΟΙ ΥΠΟΔΟΧΕΙΣ : (Ν2) Στις γραμμωτές μυϊκές ίνες (τελικές κινητικές πλάκες του Κ.Ν.Σ.
Ο παραπάνω διααχωρισμός στηρίζεται στο γεγονός ότι η μουσκαρίνη και νικοτίνη διεγείρουν τους 2 αυτούς υποδοχείς εκλεκτικά και ανεξάρτητα. Η ακετυλοχολίνη ενεργεί και στα 2 είδη υποδοχέων.
Στην προσπάθεια εξήγησης της αιτιοπαθογένειας της M.G. αναφέρονται αντισώματα, τα οποία εμφανίζουν διασταυρούμενη αντίδραση προς το υπόστρωμα των μυών του σκελετού.
Τα αντισώματα αυτά αναγνωρίζουν επιτόπους* στις πρωτεḯνες των σκελετικών μυών όπως της μυοσίνης*, ακτίνης*, ακτινίνης*.
*Επίτοπος : Τμήμα του μορίου του αντιγόνου που λειτουργεί σαν αντιγονικός καθοριστής, επιτρέποντας την σύνδεση με ειδικά αντισώματα.
*ΜΥΟΣΙΝΗ : Πρωτεḯνη η οποία βρίσκεται στα ινίδια των μυών, αποτελεί περίπου ποσοστό 45% των ολικών πρωτεϊνών του μυϊκού συστήματος. Η μυοσίνη μαζί με την ακτίνη αποτελούν τις πρωτεḯνες των μυϊκών ινών που συμμετέχουν στη συστολή του μυός. Σαν ένζυμο δρώντας η μυοσίνη απελευθερώνει ενέργεια από μόριο ΑΤΡ.
*ΑΚΤΙΝΙΝΗ : Βρίσκεται τους γραμμωτούς μύες (καρδιά – μύς σκελετού). Η α-ακτινίνη συγκροτεί τους μύες σε στρωματική διάταξη με συγκεκριμένη απόσταση μεταξύ τους.
Η μελέτη αυτών των διαφόρων αυτοαντισωμάτων στην M.G., επέδειξε και διαφορετική κλινική εικόνα του ασθενή με M.G. που εμφανίζει αυτά τα αντισώματα.
Έτσι αναφέρεται σήμερα διαχωρισμός της M.G. :
- Σε πρόωρη έναρξη M.G.
- M.G. που συνοδεύεται με αλλοιώσεις του θυμού αδένα όπως : α) υπερπλασία (ή μη ατροφία του θυμού, που επέρχεται φυσιολογικά στην ήβη. Μορφή M.G. που εμφανίζεται κατά ποσοστό 60% στις γυναίκες νεαρής ηλικίας, β) θύμωμα, όγκοι του θυμού αδένα με ποσοστό εμφάνισης 10% - 20% σε ηλικίες άνω των 40 ετών.
Γενικά η νόσος θεωρείται σαν αίτιο και εξέλιξη απορρύθμισης της φυσιολογικής λειτουργίας του ανοσοποιητικού συστήματος (σε ποσοστό 90% της γενικευμένης M.G. ανιχνεύονται αντισώματα IgG κατά της ακετυλοχολίνης, τα οποία ανευρίσκονται και σε άτομα χωρίς κλινική μυασθένεια).
Ασθενείς οι οποίοι είναι αρνητικοί στα αντισώματα ακετυλοχολίνης εμφανίζονται οροθετικοί στα αντισώματα κατά MUSK, ειδικά το γυναικείο φύλο με συχνές οφθαλμοβολβικές εντοπίσεις και κρίσεις M.G.
Είναι γνωστό ότι τα θηλέα άτομα και άτομα με ορισμένα αντιγόνα λευκοκυττάρων (HLA) εμφανίζουν προδιάθεση σε αυτοάνοσα νοσήματα.
Το “Profile” του συστήματος ιστοσυμβατότητας που περιλαμβάνει HLA-BB – HLADRW3 – HLA-DQW2 έχει αποδειχθεί ότι συνδέεται με την οφθαλμική εντόπιση της M.G.
Επίσης «κλασσικά» νοσήματα αυτοάνοσου υποστρώματος όπως ο Συστηματικός Ερυθηματώδης Λύκος (ΣΕΛ) και Ρευματοειδής Αρθρίτιδα (ΡΑ) συνυπάρχουν με M.G.
ΦΑΡΜΑΚΑ ΚΑΙ M.G.
Έχει βρεθεί ότι ορισμένα φάρμακα «προκαλούν» M.G., όπως :
- ΑΝΤΙΒΙΟΤΙΚΑ (αμινογλυκοσίδες – πολυμυξίνη – ciproxloxacin – ερυθρομυκίνη – amipicillin).
- ΠΕΝΙΚΙΛΛΑΜΙΝΗ : Μπορεί να προκαλέσει αληθή M.G. με αυξημένα anti-AChR (κατά ακετυλοχολίνη Abs) σε ποσοστό 90%. Η μυϊκή αδυναμία είναι μικρού βαθμού και η απόλυτη αποκατάσταση και υποχώρηση των συμπτωμάτων γίνεται σε εβδομάδες και μήνες μετά την διακοπή του φαρμάκου.
- Β-ΑΝΔΡΕΝΕΡΓΙΚΟΙ ΥΠΟΔΟΧΕΙΣ : Φάρμακα που «μπλοκάρουν» αυτούς (propranolol-oxprenolol).
- ΣΚΕΥΑΣΜΑΤΑ ΛΙΘΙΟΥ.
- ΣΚΕΥΑΣΜΑΤΑ Mg.
- PROCAINAMIDE
- VERAPAMIL
- QUINIDINE
- CHROLOQUINE
- PREDNISONE
- TIMOLOL (τοπικό φάρμακο γλαυκώματος)
- ΑΝΤΙΧΟΛΟΝΕΡΓΙΚΑ ΦΑΡΜΑΚΑ
- ΦΑΡΜΑΚΑ που «καταργούν» τις νευρομυϊκές συνάψεις (κουράριο – Vecuronium).
Πρέπει να χρησιμοποιούνται με πολλή προσοχή σε άρρωστο με βαρεία μυασθένεια γιατί προκαλούν παρατεταμένο νευρομυϊκό μπλοκάρισμα.
Επίσης η χορήγηση Nitrofuriutoin έχει ενοχοποιηθεί για την εκδήλωση οφθαλμικής M.G.
Διακοπή του φαρμάκου οδηγεί σε πλήρη αποκατάσταση.
ΣΧΕΣΗ ΤΟΥ ΘΥΜΟΥ ΑΔΕΝΑ ΜΕ M.G.
Ο ΘΥΜΟΣ ΑΔΕΝΑΣ έχει μέγεθος κατά την γέννηση 5cm μήκος – 4cm πλάτος – 6cm πάχος – βάρος 20-37gr στην εφηβεία.
Μετά συρρικνώνεται και δεν διαφοροποιείται από τον περιβάλλοντα λιπώδη ιστό (σε άτομο 75 ετών ζυγίζει 6gr).
Ετυμολογικά η λέξη ΘΥΜΟΣ προέρχεται από τους Έλληνες (ΘΥΜΟΣ : οργή, καρδιά, ψυχή, επιθυμία) και η ονομασία του προέρχεται πιθανώς από την ανατομική θέση του θυμού αδένα στον θώρακα (κοντά στην καρδιά) όπου αναπτύσσονται όλα τα υποκειμενικά συναισθήματα).
Ο Γαληνός ήταν ο πρώτος ο οποίος παρατήρησε ότι ο θυμός αδένας μεταβάλλει το μέγεθος του κατά τη διάρκεια της ζωής του κάθε ατόμου. Επίσης το έτος 1961 ο Jacques Miller (ανακαλύπτει τη σημασία του θυμού αδένα και ενεργό συμμετοχεί του στο ανοσοποιητικό σύστημα του ανθρώπου.
Ο θυμός αποτελεί τόπο ωρίμανσης των Τ-κυττάρων αλλά και επιλογής αυτών (Τ-κύτταρα λειτουργικά > θετική επιλογή, εξάλειψη αυτοαντιδραστικών Τ-Κυττάρων > αρνητική επιλογή).
Τα κύτταρα του θυμού που προκύπτουν από τις δύο αυτές επιλογές εισέρχονται στην κυκλοφορία του αίματος και αποτελούν πλέον ζωτικά στοιχεία λειτουργίας του ανοσοποιητικού συστήματος.
Οι ανωμαλίες του θυμού αδένα βρίσκονται συχνά στη M.G.
Έτσι 85% των ασθενών με M.G. εμφανίζουν υπερπλασία του θυμού αδένα 10% - 15% έχουν θύμωμα.
Υπερθυρεοειδισμός συνοδεύει σε ποσοστό 3 – 8% την M.G. (την «οφθαλμική» εντόπιση της M.G.).
ΚΛΙΝΙΚΑ ΣΗΜΕΙΑ Μ.G.
Αδυναμία των οφθαλμικών μυών και πτώση των βλεφάρων εμφανίζονται σε ποσοστό 50% των ασθενών με M.G.
Συνοδεύει 90% την εξελικτική πορεία της νόσου.
Επίσης οι μύς του τράχηλου πάσχουν με αποτέλεσμα αδυναμία κάμψης, έκτασης του κεφαλιού.
Γενικευμένη μυϊκή αδυναμία των άκρων (εγγύς μυϊκών μαζών κυρίως).
Μονήρης μυϊκή αδυναμία (μία ομάδα μυών) σπάνια προβάλλεται στη M.G. (ποσοστό λιγότερο 10%).
Η μυϊκή αδυναμία που χαρακτηρίζει τη M.G. τείνει να επεκταθεί από την περιοχή των μυών οφθαλμών και του προσώπου, τράχηλου, στον κορμό και κάτω άκρα.
Υπάρχουν περιπτώσεις όπου η νόσος περιορίζεται στους μυς οφθαλμού για πολλά χρόνια (ποσοστό 10%).
Ποσοστό 87% των ασθενών με M.G. εμφανίζουν γενικευμένο νόσημα εντός 13 μηνών από την έναρξη της νόσου.
Στά άτομα με γενικευμένη M.G. με έντονο ηλιακό φώς – χειρουργικές επεμβάσεις – εμβολιασμούς – συναισθηματικό stress – εμμηνορρυσία προκαλούν έξαρση της νόσου.
Επίσης λοιμώξεις (εποχιακές ιώσεις), χορήγηση φαρμάκων (βλέπε παραπάνω) επιδεινώνουν την μυϊκή αδυναμία της M.G. και οδηγούν σε κρίση μυασθένειας* και συμμετοχή του αναπνευστικού συστήματος.
*Κρίση μυασθένειας : οφείλεται σε παραγωγή ακετυλοχολίνης στην τελική κινητική πλάκα. Προκαλείται από χορήγηση υπερβολική ανταγωνιστών ακετυλοχολίνης – κατά τις χειρουργικές επεμβάσεις.
Αυτόματες υφέσεις σπάνια συμβαίνουν στη M.G.
Μακράς διάρκειας, ολοκληρωτικές υφέσεις είναι πολύ σπάνιες.
Υφέσεις με κατάλληλη θεραπεία παρατηρούνται κατά τα πρώτα 3 χρόνια από την έναρξη της νόσου.
Η Αμερικανική ένωση για την M.G. προτείνει διαιρέσεις της M.G., που διευκολύνουν γιατρό και άρρωστο.
ΤΑΞΗ Ι M.G. |
|
ΤΑΞΗ IΙ M.G. |
|
ΤΑΞΗ ΙIa M.G. |
|
ΤΑΞΗ ΙIb M.G. |
|
ΤΑΞΗ ΙII M.G. |
|
Συχνότητα εμφάνισης της M.G. είναι 2/100.000 στις ΗΠΑ και 15/100.000 πληθυσμό της Αγγλίας.
Τελευταία παρατηρείται αύξηση (0,5 – 14.2 περιπτώσεις στα 100.000 άτομα). Η αύξηση αυτή θεωρείται ότι οφείλεται στην επιμήκυνση του χρόνου ζωής των ασθενών με M.G. αλλά και στην δυνατότητα πρόωρης διάγνωσης της νόσου. Αναλογία M.G./θηλέος/αρρένα 3:2. Ο χρόνος εμφάνισης M.G. είναι 28 χρόνια στις γυναίκες και 42 χρόνια στους άνδρες. Η M.G. της νεαρής ηλικίας είναι περισσότερο κοινή στους Ασιάτες.
Η M.G. μπορεί να εμφανιστεί στα παιδιά των εγκύων γυναικών που έχουν τη νόσο. Οφείλεται σε μεταφορά IgG αντισωμάτων κατά της ακετυλοχολίνης (anti-AchR) μέσω του πλακούντα της μήτρας. Τα νεογνά των οποίων οι μητέρες εμφανίζουν anti-AchR έχουν ποσοστό M.G. 10-20% που θεωρείται μικρό. Αυτό αποδίδεται στην «προστατευτική» ενέργεια της a-fetoprotein που εμποδίζει την σύνδεση του αντισώματος κατά της ακετυλοχολίνης.
Η μείωση των υψηλών τίτλων αντισωμάτων κατά της ακετυλοχολίνης σε έγκυο γυναίκα με τη μέθοδο της πλασμαφαίρεσης μειώνει τις πιθανότητες εμφάνισης M.G. στο νεογνό.
ΣΤΟΙΧΕΙΑ ΑΝΑΤΟΜΙΚΗΣ ΦΥΣΙΟΛΟΓΙΑΣ
Στην M.G. αυτοαντισώματα (ανοσοσφαιρίνη G – IgG) αναπτύσσονται κατά των προσυναπτικών νικοτινικών υποδοχέων που βρίσκονται στις νευρομυϊκές συνάψεις.
Ο λόγος της εμφάνισης των αυτοαντισωμάτων είναι άγνωστος, έχει βέβαια εξακριβωθεί ότι ορισμένοι γονότυποι ανθρώπων είναι πιο «ευαίσθητοι» στο να αναπτύσουν τα αντισώματα αυτά.
Η φυσιολογική και παθολογική λειτουργία της νευρομυϊκης σύναψης όπως και η λειτουργία της στην μυασθένεια gravis (M.G.) απεικονίζεται στον Πίνακα 2.
Πίνακας 2
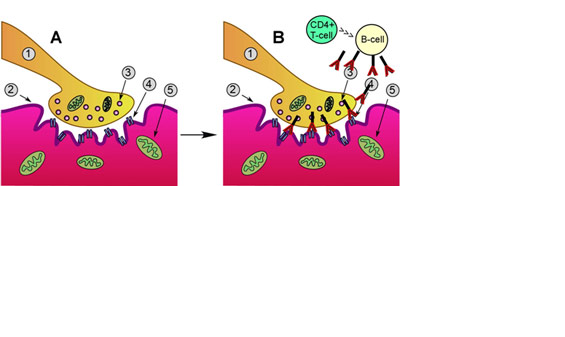
Α. Φυσιολογική νευρομυϊκή σύναψη
Ερεθίσματα μεταδίδονται από την απόληξη του κινητικού νεύρου (1) μέσω απελευθέρωσης του νευροδιαβιβαστή ακετυλοχολίνη (3) στη περιοχή μεταξύ του νεύρου και του μυός (2). Στη πλευρά του μυός η ακετυλοχολίνη συναντά τους υποδοχείς της (4) οι οποίοι μεταδίδουν το ερέθισμα στους μύες (5) με αποτέλεσμα την εκούσια κίνηση των μυών.
Β. Ασθενής με M.G. όπου μη φυσιολογική δραστηριοποίηση κυττάρων του ανοσοποιητικού συστήματος CD4 + T cell + B cell οδηγεί στη παραγωγή Abs έναντι των υποδοχέων ακετυλοχολίνης, που έχει σαν αποτέλεσμα να μην είναι δυνατή η μετάδοση του ερεθίσματος από το νεύρο στους μύες και τελικά αδυναμία των μυών.
Οι υποδοχείς της ακετυλοχολίνης αποτελούνται από 5 υποομάδες (2 αλφα – 1 βήτα – 1 γάμμα – 1 δέλτα). Βλέπε πίνακα 1.
Αυτές είναι ομόλογες στα διάφορα είδη θηλαστικών, αποδεικνύοντας ότι τα γονίδια που κωδικάρουν αυτά προέρχονται από κοινό αρχέγονο γονίδιο.
Υποδοχείς ακετυλοχολίνης υπάρχουν σε όλη την επιφανειακή μεμβράνη των μυών με υψηλή συγκέντρωση στις άκρες των νευρομυϊκών συνάψεων.
Όταν ένα μόριο ακετυλοχολίνης συνδέεται με τον ειδικό υποδοχέα αυτός ο υποδοχέας υφίσταται άμεσα τρισδιάστατη διαμορφωτική μεταβολή με αποτέλεσμα άνοιγμα του καναλιού ιόντων.
Φυσιολογικά τα άκρα των προσυναπτικών νευρών περιέχουν κυστίδια γεμάτα με ακετυλοχολίνη.
Όταν ένα ερέθισμα ερεθίζει το κινητικό νεύρο, φτάνοντας στο τελικό άκρο του τα περιεχόμενα των κυστιδίων απελευθερώνονται στην συναπτική πλάκα μέσω επίδρασης ιόντων Ca.
Τα μόρια της ακετυλοχολίνης διαχέονται κατά μήκος της σύναψης και συνδέονται με τους υποδοχείς της ακετυλοχολίνης σε όλη την προσυναπτική μεμβράνη, προκαλώντας απελευθέρωση ιόντων Νατρίου και αποπόλωση της προσυναπτικής μεμβράνης με τελική κατάληψη τη συστολή του μυός (βλέπε Πίνακα 3).
Πίνακας 3
Φυσιολογική νευρομυϊκή ζεύξη που δείχνει μία προσυναπτική απόληξη με κινητικό νεύρο που καταλήγει σε διόγνωση (mouton terminale) ΤΕΛΙΚΗ ΚΙΝΗΤΙΚΗ ΠΛΑΚΑ.
Synaptic cleft + postsynaptic membrane με πολλαπλές fods +
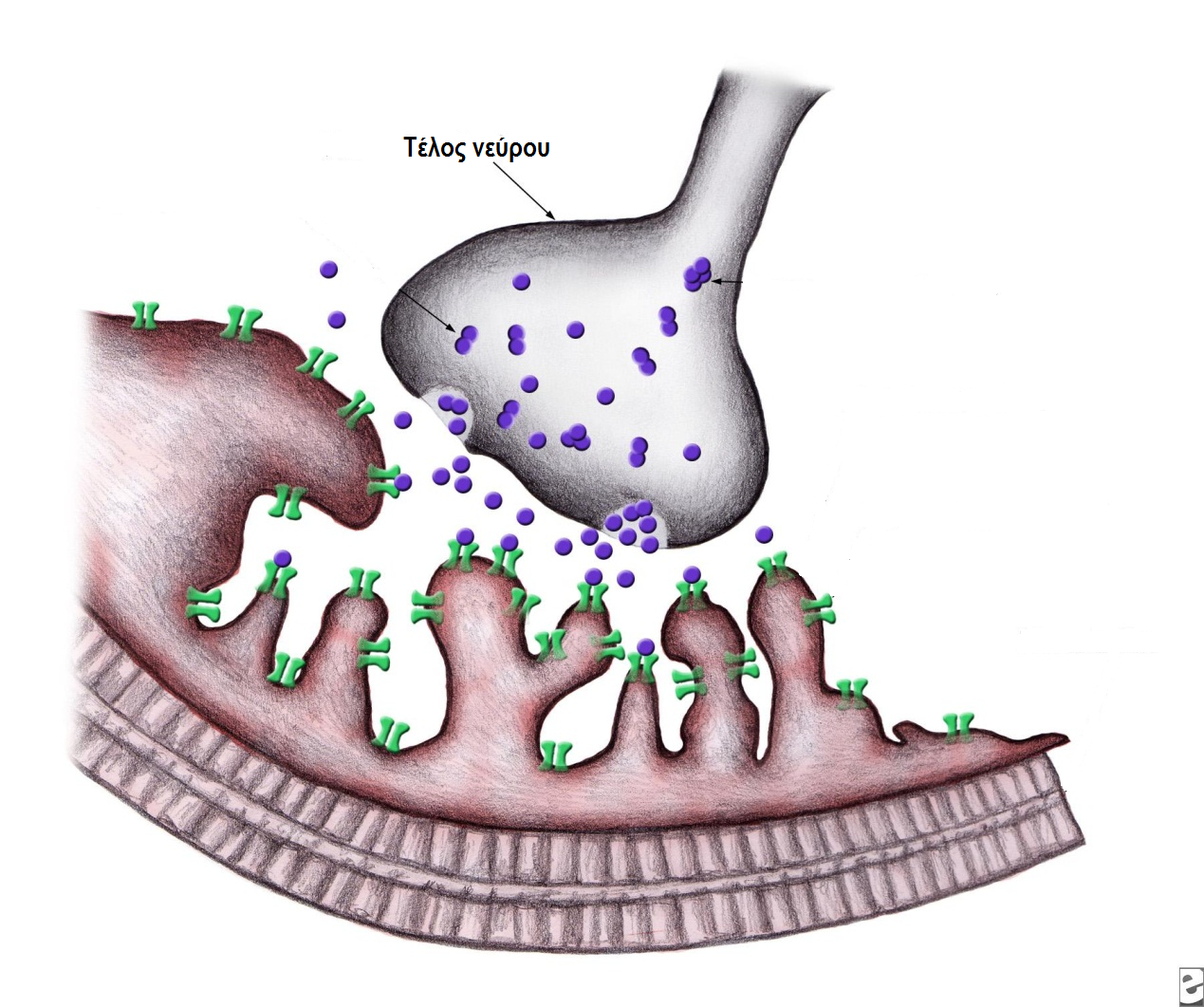
Με κάθε ερεθισμό νεύρου, ποσότητα ακετυλοχολίνης ελευθερώνεται από τον προσυναπτικό κινητικό νεύρωνα που παροδικά υφίσταται μείωση των αποθηκών της υπάρχουσας ακετυλοχολίνης (προσυναπτική έλλειψη). Στην περίπτωση ης βαρείας μυασθένειας αφ’ ενός ανεπαρκής νευρομυϊκός ερεθισμός και αφ’ ετέρου το φυσιολογικό φαινόμενο της «προσυναπτικής έλλειψης» έχει σαν αποτέλεσμα την μείωση ενεργοποίησης μεγάλου αριθμού μυϊκών ινών.
Αυτό κλινικά εκφράζεται με την μυϊκή αδυναμία και κόπωση στον ασθενή που πάσχει από βαρεία μυασθένεια.
Τα άτομα με M.G. εμφανίζουν συμπτώματα όταν ο συνολικός αριθμός των υποδοχέων τους ακετυλοχολίνης αγγίζει ποσοστό 30% του κανονικού.
Οι χολινεργικοί υποδοχείς που φυσιολογικά υπάρχουν στους μυς της καρδιάς διαθέτουν διαφορετική αντιγονικότητα* από τους μυς τους σκελετού και δεν επηρεάζονται στο αρχικό αυτό στάδιο.
*Αντιγονικότητα : Η κατάσταση κατά την οποία κάποιο ερέθισμα μπορεί να προκαλέσει αντισωματική απάντηση (δημιουργία αντισώματος).
Οι ακριβείς μηχανισμοί που προκαλούν απώλεια της ανοσολογικής ανοχής* δρα το μόριο την ακετυλοχολίνης και δημιουργία αυτοαντισώματος δεν είναι απόλυτα εξακριβωμένοι. Τα Β κύτταρα βεβαίως συμμετέχουν αλλά και τα Τ-κύτταρα, εξαρτώμενη χυμική ανοσία είναι εμφανής (ρόλος θύμου – ανωμαλίες αυτού θύμωμα – όγκοι στη M.G.).
*Ανοσολογικη ανοχή : Η κατάσταση κατά την οποία το φυσιολογικό ανοσολογικό σύστημα δεν αντιδρά στα αντιγόνα του ίδιου σώματος. Προκαλείται από μηχανισμό που «καταστρέφουν» τα λεμφοκύτταρα.
ΚΛΙΝΙΚΑ ΣΗΜΕΙΑ – ΣΥΜΠΤΩΜΑΤΑ M.G.
- Πρωταρχικό και πιο κοινό σύμπτωμα είναι μυϊκη αδυναμία.
- Πτώση βλεφάρου, αδυναμία οφθαλμικών μυών εμφανίζεται σε ποσοστό 50% των αρρώστων, ενώ συνοδεύει την πορεία της νόσου σε ποσοστό 90%.
- Η οφθαλμική εντόπιση της νόσου (σαν σύμπτωμα) περιορίζεται στο 16% του συνόλου των ασθενών.
- Η αδυναμία των άκρων αφορά κυρίως τις εγγύς ομάδες μυών.
- Μυϊκή αδυναμία ομάδες μεμονωμένων μυών, εμφανίζεται σε ποσοστό μικρότερο του 10%, του συνόλου.
- Η αδυναμία και μυϊκή κόπωση εμφανίζεται λιγότερη σοβαρή το πρωϊ και επιδεινώνεται με την πρόοδο της ημέρας. Η αδυναμία αυτή επιδεινώνεται με την σωματική άσκηση και βελτιώνεται με την ανάπαυση. Επίσης εμφανίζει προοδευτική επιδείνωση με την πάροδο του χρόνου (εβδομάδες, μήνες) με εξάρσεις και υφέσεις.
- Ποσοστό 87% των ασθενών με M.G. εμφανίζουν γενίκευση νόσου εντός 13 μηνών από την έναρξη αυτής.
Όπως ήδη αναφέρθηκε διάφοροι εξωγενείς παράγοντες, όπως :
- Έντονη ηλιακή ακτινοβολία.
- Χειρουργικές επεμβάσεις.
- Φάρμακα (αμινογλυκοσίδες – κινολόνες – χλωροκίνη – προκαϊνη – σκευάσματα λιθίου – B αναστολείς – στατίνες) επιτείνουν την συμπτωματολογία και πορεία της Βαρείας Μυασθένειας (M.G.).
ΔΙΑΓΝΩΣΗ ΒΑΡΕΙΑΣ ΜΥΑΣΘΕΝΕΙΑΣ (M.G.)
Η ανεύρεση αντισωμάτων κατά των υποδοχέων της ακετυλοχολίνης αποτελεί κύριο διαγνωστικό όπλο για την M.G. με τα εξής δεδομένα :
- Υψηλή ειδικότητα (~100%)
- Θετικά σε γενικευμένη μορφή της M.G.
- Θετικά στο 50-70% των ασθενών με οφθαλμική εκδήλωση M.G.
Ψευδώς θετικά έχουν βρεθεί :
- Θύμωμα χωρίς M.G.
- Σύνδρομο Lambert-Eaton*
- Μικροκυτταρικό Ca πνευμόνων
- Θεραπεία πενικιλλαμίνης στην Ρευματοειδή αρθρίτιδα.
- Σε ποσοστό 1-3% σε άτομα άνω των 70 ετών.
*Σύνδρομο Lambert-Eaton
Μυασθενικό σύνδρομο Lambert-Eaton : Αυτοάνοσο νόσημα στο οποίο παρατηρείται αδυναμία των εγγύς μυϊκών ομάδων (ωμική ζώνη – ισχίο), μειωμένα ανταννακλαστικά και δυσλειτουργία του αυτόνομου νευρικού συστήματος.
Το σύνδρομο παρατηρείται στον μικροκυτταρικό καρκίνωμα πνευμόνων και σε άλλες νεοπλασίες.
Για την ολοκλήρωση της διάγνωσης πρέπει να αναζητηθούν επίσης :
- Αντισώματα κατά anti-MUSK (βρίσκονται στο 50% των ασθενών με αρνητικά anti- ακετυλίνης αντισώματα).
- Anti Agrin αντίσωμα.
- Σε άτομα με θύμωμα και M.G. αντισώματα κατά Ραβδοτών μυών αλλά σε ασθενείς με M.G. ηλικίας άνω των 50 ετών.
Βοηθητικές εξετάσεις :
- C.T. θώρακος (αναζήτηση θυμώματος).
- Σε οφθαλμική μορφή M.G. M.R.I. εγκεφάλου, οφθαλμού για εξακρίβωση ογκόμορφων αλλοιώσεων που πιέζουν το οφθαλμικό νεύρο ή στέλεχος εγκεφάλου.
- Ηλεκτρομυογράφημα και ταχύτητα αγωγής ερεθίσματος παρέχουν πληροφορίες για την κατάσταση των μυϊκών ομάδων στην M.G.
ΘΕΡΑΠΕΙΑ
Οι πρόσφατες έρευνες και ερμηνεία των αντισωμάτων που χαρακτηρίζουν την M.G. έχουν διαχωρίσει τις διάφορες θεραπείες (διαχωρισμός ασθενών με M.G. σε υποομάδες, ανάλογα με τα αντισώματα που ανιχνεύονται και την κλινική εικόνα αυτών, την έναρξη της νόσου, συνύπαρξη M.G. με θύμωμα, οφθαλμική εντόπιση της M.G.
Έτσι, η θεραπεία της M.G. περιλαμβάνει :
- ΑΝΑΣΤΟΛΕΙΣ ΤΗΣ ΑΝΤΙ-ΧΟΛΙΝΕΣΤΕΡΑΣΗΣ
- ΑΝΟΣΟΡΥΘΜΙΣΤΙΚΟΥΣ ΠΑΡΑΓΟΝΤΕΣ
- ΕΝΔΟΦΛΕΒΙΑ ΧΟΡΗΓΗΣΗ Ανοσοσφαιρίνης
- ΠΛΑΣΜΑΦΑΙΡΕΣΗ
- ΘΥΜΕΚΤΟΜΗ.
ΑΝΑΣΤΟΛΕΙΣ ΑΝΤΙ-ΧΟΛΙΝΕΣΤΕΡΑΣΗΣ
- Αρχική θεραπεία για μέτρια M.G.
- Φυσοστιγμίνη χορηγείται σαν θεραπεία συντήρησης.
- Κορτικοειδή : ελάχιστη ωφέλεια.
- Ουζαθειαπρίνη μετά από χορήγηση κορτικοειδών.
- Κυκλοσπορίνη Α – Μεθοτρεξίδη – Κυκλοφωσφαιμίδη (σοβαρές μορφές M.G.).
ΠΛΑΣΜΑΦΑΙΡΕΣΗ
- Για την κρίση μυασθένειας και ανθεκτική μορφή M.G.
- Σαν προπαρασκευή για χειρουργικές επεμβάσεις.
- Βελτίωση σημειώνεται βραχύχρονης διάρκειας (~ 2μήνες).
- Περιοδική εφαρμογή κατά εβδομάδα ή μήνα και μετά την αποτυχία των άλλων θεραπειών.
ΘΥΜΕΚΤΟΜΗ
- Άτομα ηλικίας 10-55 ετών σε ασθενείς με θύμωμα αλλά και σε ασθενείς χωρίς θύμωμα αλλά γενικευμένης μορφής M.G.
- Πρώτη γραμμή θεραπείας στη γενικευμένη M.G.
- Στην οφθαλμική εντόπιση της M.G. μπορεί να υπάρξη αναμονή 2 ετών, μήπως προκύψει αυτόματη ύφεση.
- Δεν συνιστάται σε άτομα με M.G. εμφανίζουν αντισώματα στον ορό του αίματος κατά κινάσης των μυών.
ΔΟΚΙΜΑΣΙΑ ΠΑΓΟΥ
- Ειδικά για την οφθαλμολογική εντόπιση M.G.
- Η τοποθέτηση πάγου στο βλέφαρο που εμφανίζει M.G. προκαλεί βελτίωση (βελτιώνει την πτώση του βλεφάρου και την διπλωπία που προκαλεί η M.G.). Πιθανώς η εφαρμογή της κρύας επιφάνειας του παγόκυβου βελτιώνει την νευρομυϊκή διαβίβαση.
ΠΡΟΓΝΩΣΗ Μ.G.
Η θεραπεία με τα φάρμακα που αναφέρθηκαν όπως και η υποστηρικτική αρωγή της μονάδας εντατικής θεραπείας εξασφαλίζει αξιοπρεπή ζωή στον ασθενή με M.G.
Θνητότητα M.G. : 3% - 4% επικίνδυνοι παράγοντες :
- Μεγάλη ηλικία > 40 ετών.
- Ελλειπή θεραπεία M.G.
- Παρουσία θυμώματος.
Όλα τα παραπάνω διαγράφουν τον κλασσικό ορισμό βαρεία της νόσου.
Προηγούμενη θνητότητα ασθενών με M.G. άγγιζε το 30% - 40%.
Η σημερινή προβληματική επιπλοκή της M.G. είναι η εντόπιση στους μυς της αναπνοής, που πιθανόν να καταλήξει σε μηχανική υποστήριξη.
ΔΙΑΦΟΡΙΚΗ ΔΙΑΓΝΩΣΗ ΤΗΣ ΒΑΡΕΙΑΣ ΜΥΑΣΘΕΝΕΙΑΣ, γίνεται από:
- Αλλαντίαση
- Συμπιέσεις κρανιακών νεύρων
- Κατάθλιψη
- Εκ φαρμάκων προκαλούμενα μυασθενικά σύνδρομα (αντιβιωτικά : κινολόνες – πενικιλλίνη – ερυθρομυκίνη – αμπικιλλίνη – πολυμιξίνη – αμινογλυκοσίδες – αναστολείς β υποδοχέων – προκαϊναμίδη – βεραπαμίδη – κινιδίνη – στατίνες).
Ref. : - Medscape
- Merck Man 19th ed.
- Taber’s Ιατρ. Λεξικό




